Neue Technik durchbricht eine Technologie-Barriere, die die RNA-Bildgebung 50 Jahre lang einschränkte
Forscher entwickeln Werkzeuge zur Schärfung der 3D-Ansicht von großen RNA-Molekülen
Wissenschaftler der University of Maryland haben eine Methode entwickelt, um die Strukturen von großen RNA-Molekülen mit hoher Auflösung zu bestimmen. Die Methode überwindet eine Herausforderung, die in den letzten 50 Jahren die 3D-Analyse und Abbildung von RNA auf nur kleine Moleküle und RNA-Stücke beschränkt hat.
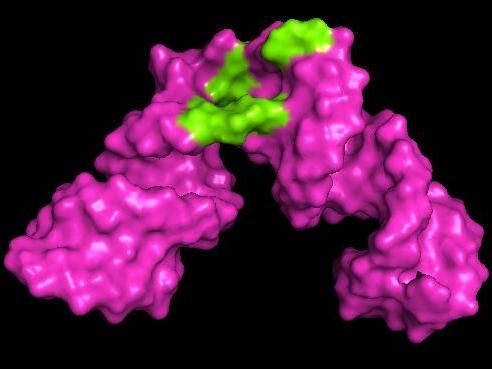
Forscher der University of Maryland entwickelten eine Methode zur Erweiterung des Anwendungsbereichs der kernmagnetischen Resonanzspektroskopie (NMR-Spektroskopie). Im obigen Beispiel konnten die Forscher ein 3D-Bild erstellen, das die Stelle auf einem Stück Hepatitis-RNA zeigt, an der sich kleine Moleküle wie z.B. ein Medikament binden könnten (grün dargestellt).
Kwaku Dayie/University of Maryland
Die neue Methode, die den Anwendungsbereich der kernmagnetischen Resonanzspektroskopie (NMR) erweitert, wird es den Forschern ermöglichen, die Form und Struktur von RNA-Molekülen zu verstehen und zu lernen, wie sie mit anderen Molekülen interagieren. Die durch diese Technologie gewonnenen Erkenntnisse könnten zu gezielten RNA-Therapiebehandlungen von Krankheiten führen. Das Forschungspapier zu dieser Arbeit wurde am 7. Oktober 2020 in der Zeitschrift Science Advances veröffentlicht.
"Das Gebiet der kernmagnetischen Resonanzspektroskopie ist steckengeblieben, wenn man Dinge betrachtet, die klein sind, sagen wir 35 RNA-Bausteine oder Nukleotide. Aber die meisten der interessanten Dinge, die biologisch und medizinisch relevant sind, sind viel größer, 100 Nukleotide oder mehr", sagte Kwaku Dayie, Professor für Chemie und Biochemie an der UMD und Seniorautor der Arbeit. "Es ist also sehr aufregend, in der Lage zu sein, den Stau aufzulösen und die großen Dinge zu betrachten. Es wird uns erlauben, in diese Moleküle hineinzuschauen und zu sehen, was in einer Weise vor sich geht, wie wir es bisher nicht konnten.
Bei der NMR-Spektroskopie richten die Wissenschaftler Radiowellen auf ein Molekül, regen die Atome an und "beleuchten" das Molekül. Durch die Messung von Veränderungen im Magnetfeld um die angeregten Atome herum - der kernmagnetischen Resonanz - können die Wissenschaftler Eigenschaften wie Form, Struktur und Bewegung des Moleküls rekonstruieren. Die dabei gewonnenen Daten können dann zur Erzeugung von Bildern verwendet werden, ähnlich wie MRT-Bilder in der Medizin.
Normalerweise überschneiden sich die NMR-Signale der vielen Atome in einem biologischen Molekül wie der RNA miteinander, was die Analyse sehr schwierig macht. In den 1970er Jahren lernten die Wissenschaftler jedoch, RNA-Moleküle biochemisch so zu verändern, dass sie besser mit NMR arbeiten, indem sie die Wasserstoffatome durch magnetisch aktive Fluoratome ersetzten. In relativ kleinen RNA-Molekülen, die aus 35 oder weniger Nukleotiden bestehen, leuchten die Fluoratome leicht auf, wenn sie von Radiowellen getroffen werden, und bleiben lange genug für eine hochauflösende Analyse angeregt. Wenn die RNA-Moleküle jedoch größer werden, leuchten die Fluoratome nur kurz auf und verlieren dann schnell ihr Signal. Dies hat eine hochauflösende 3D-Analyse von größeren RNA-Molekülen verhindert.
Frühere Arbeiten von anderen hatten gezeigt, dass Fluor weiterhin ein starkes Signal erzeugt, wenn es sich neben einem Kohlenstoffatom mit sechs Protonen und sieben Neutronen (C-13) befindet. Also entwickelten Dayie und sein Team eine relativ einfache Methode, um das natürlich vorkommende C-12 in der RNA (die 6 Protonen und 6 Neutronen enthält) in C-13 umzuwandeln und ein Fluoratom (F-19) direkt daneben zu installieren.
Dayie und sein Team zeigten zunächst, dass ihre Methode Daten und Bilder erzeugen konnte, die den heutigen Methoden gleichwertig sind, indem sie sie auf RNA-Stücke von HIV mit 30 Nukleotiden anwandten, die zuvor abgebildet worden waren. Dann wendeten sie ihre Methode auf RNA-Stücke von Hepatitis B an, die 61 Nukleotide enthielten - fast doppelt so gross wie die vorher für RNA mögliche NMR-Spektroskopie.
Ihre Methode ermöglichte es den Forschern, Stellen auf der Hepatitis-B-RNA zu identifizieren, an denen kleine Moleküle an die RNA binden und mit ihr interagieren. Das könnte nützlich sein, um die Wirkung potenzieller therapeutischer Medikamente zu verstehen. Der nächste Schritt für die Forscher ist die Analyse noch größerer RNA-Moleküle.
"Diese Arbeit erlaubt es uns, das zu erweitern, was in den Fokus gerückt werden kann", sagte Dayie. "Unsere Berechnungen sagen uns, dass wir theoretisch wirklich große Dinge betrachten können, wie einen Teil des Ribosoms, der molekularen Maschine, die im Inneren der Zellen Proteine synthetisiert.
Durch das Verständnis der Form und Struktur eines Moleküls können Wissenschaftler seine Funktion und die Wechselwirkungen mit seiner Umgebung besser verstehen. Darüber hinaus wird diese Technologie es den Wissenschaftlern ermöglichen, die 3D-Struktur zu sehen, während sie sich verändert, da insbesondere RNA-Moleküle häufig ihre Form ändern. Dieses Wissen ist der Schlüssel zur Entwicklung von Therapeutika, die gezielt auf krankheitsspezifische Moleküle abzielen, ohne gesunde Zellfunktionen zu beeinträchtigen.
"Die Hoffnung ist, dass die Forscher, wenn sie die Schlupfwinkel in einem gestörten Molekül kennen, Medikamente entwickeln können, die die Schlupfwinkel ausfüllen, um es außer Gefecht zu setzen", sagte Dayie. "Und wenn wir diesen Molekülen folgen können, während sie ihre Form und Struktur verändern, dann wird ihre Reaktion auf potenzielle Medikamente etwas besser vorhersagbar sein, und die Entwicklung wirksamer Medikamente kann effizienter sein.
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Spektroskopie
Durch die Untersuchung mit Spektroskopie ermöglicht uns einzigartige Einblicke in die Zusammensetzung und Struktur von Materialien. Von der UV-Vis-Spektroskopie über die Infrarot- und Raman-Spektroskopie bis hin zur Fluoreszenz- und Atomabsorptionsspektroskopie - die Spektroskopie bietet uns ein breites Spektrum an analytischen Techniken, um Substanzen präzise zu charakterisieren. Tauchen Sie ein in die faszinierende Welt der Spektroskopie!

Themenwelt Spektroskopie
Durch die Untersuchung mit Spektroskopie ermöglicht uns einzigartige Einblicke in die Zusammensetzung und Struktur von Materialien. Von der UV-Vis-Spektroskopie über die Infrarot- und Raman-Spektroskopie bis hin zur Fluoreszenz- und Atomabsorptionsspektroskopie - die Spektroskopie bietet uns ein breites Spektrum an analytischen Techniken, um Substanzen präzise zu charakterisieren. Tauchen Sie ein in die faszinierende Welt der Spektroskopie!

























































