Heranzoomen, um das ganze Bild zu sehen
Forscher nutzen Einzelzellansätze und Deep Learning, um alle Stadien der Embryonalentwicklung von Fruchtfliegen abzubilden, und kommen damit möglicherweise der prädiktiven Embryonengenomik einen Schritt näher
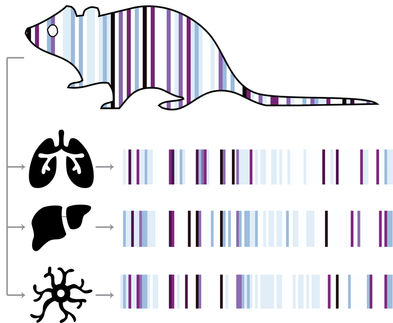
Wissenschaftler haben mit der Fruchtfliege als Modellorganismus die bisher vollständigste und detaillierteste Einzelzellkarte der Embryonalentwicklung in einem Tier erstellt .
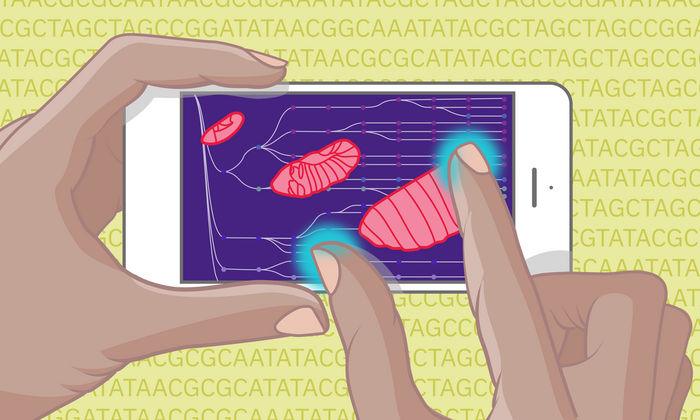
Ein neuer Atlas, der das Kontinuum der Embryonalentwicklung bei Fruchtfliegen abbildet, geht dank maschinellem Lernen noch weiter
Isabel Romero Calvo/EMBL
Die in der Fachzeitschrift Science veröffentlichte Studie unter der Leitung von Eileen Furlong am EMBL und Jay Shendure von der University of Washington nutzt die Daten von mehr als einer Million embryonaler Zellen, die alle Stadien der Embryonalentwicklung abdecken, und stellt auf mehreren Ebenen einen bedeutenden Fortschritt dar. Diese Grundlagenforschung hilft den Wissenschaftlern auch bei der Beantwortung der Frage, wie Mutationen zu verschiedenen Entwicklungsstörungen führen. Darüber hinaus eröffnet sie einen Weg zum Verständnis des riesigen nicht codierenden Teils unseres Genoms, der die meisten krankheitsbedingten Mutationen enthält.
"Allein die Erfassung der gesamten Embryogenese - aller Stadien und aller Zelltypen - um ein vollständigeres Bild der Zellzustände und molekularen Veränderungen zu erhalten, die die Entwicklung begleiten, ist schon eine Leistung für sich", sagt Eileen Furlong, Leiterin der Abteilung Genombiologie am EMBL. "Aber was mich wirklich begeistert, ist der Einsatz von Deep Learning, um einen kontinuierlichen Überblick über die molekularen Veränderungen zu erhalten, die die Embryonalentwicklung vorantreiben - und zwar bis ins kleinste Detail."
Die Embryonalentwicklung beginnt mit der Befruchtung einer Eizelle, gefolgt von einer Reihe von Zellteilungen und Entscheidungen, aus denen ein sehr komplexer multizellulärer Embryo hervorgeht, der sich bewegen, essen, fühlen und mit seiner Umgebung interagieren kann. Forscher untersuchen diesen Prozess der Embryonalentwicklung seit über hundert Jahren, aber erst im letzten Jahrzehnt haben neue Technologien es den Wissenschaftlern ermöglicht, die molekularen Veränderungen, die die Zellübergänge begleiten, auf der Ebene einzelner Zellen zu identifizieren.
Diese Einzelzellstudien haben große Begeisterung ausgelöst, da sie die Komplexität der Zelltypen in den Geweben aufzeigten, sogar neue Zelltypen identifizierten und ihre Entwicklungswege zusätzlich zu den zugrunde liegenden molekularen Veränderungen aufzeigten. Versuche, die gesamte Embryonalentwicklung in Einzelzellauflösung zu erfassen, waren jedoch aufgrund zahlreicher technischer Herausforderungen bei der Probenahme, den Kosten und den Technologien unerreichbar.
In dieser Hinsicht hat die Fruchtfliege(Drosophila melanogaster), ein herausragender Modellorganismus in der Entwicklungsbiologie, Genregulation und Chromatinbiologie, einige entscheidende Vorteile, wenn es darum geht, neue Ansätze zu entwickeln, um dieses Problem anzugehen. Die Embryonalentwicklung der Fruchtfliege verläuft extrem schnell; innerhalb von nur 20 Stunden nach der Befruchtung haben sich alle Gewebe gebildet, einschließlich des Gehirns, des Darms und des Herzens, so dass der Organismus krabbeln und essen kann. Dies und die vielen Entdeckungen, die bei Fruchtfliegen gemacht wurden und das Verständnis der Funktionsweise von Genen und ihren Produkten vorantrieben, ermutigten das Furlong-Labor und seine Mitarbeiter, sich dieser Herausforderung zu stellen.
"Unser Ziel war es, einen kontinuierlichen Überblick über alle Stadien der Embryogenese zu erhalten, um die gesamte Dynamik und die Veränderungen während der Entwicklung eines Embryos zu erfassen, und zwar nicht nur auf der Ebene der RNA, sondern auch der Steuerelemente, die diesen Prozess regulieren", so Co-Autor Stefano Secchia, Doktorand in der Furlong-Gruppe.
Vorläufige Arbeit mit 'Enhancern'
Im Jahr 2018 haben die Gruppen Furlong und Shendure gezeigt, dass es möglich ist, "offenes" Chromatin mit Einzelzellauflösung in Embryonen zu profilieren, und dass diese DNA-Regionen oft aktive Entwicklungsverstärker darstellen. Enhancer" sind DNA-Abschnitte, die als Kontrollschalter fungieren und Gene ein- und ausschalten. Die Daten zeigen, welche Zelltypen im Embryo zu einem bestimmten Zeitpunkt welche Enhancer nutzen und wie sich diese Nutzung im Laufe der Zeit verändert. Eine solche Karte ist wichtig, um zu verstehen, was bestimmte Aspekte der Embryonalentwicklung antreibt.
"Ich war wirklich begeistert, als ich diese Ergebnisse sah", sagte Furlong. "Dass wir über die RNA hinausgehen und uns diese regulatorischen Schalter in einzelnen Zellen ansehen können, hätte ich lange nicht für möglich gehalten."
Mehr als nur "Schnappschüsse
Die Studie aus dem Jahr 2018 war zu diesem Zeitpunkt auf dem neuesten Stand der Technik und erstellte Profile von etwa 20.000 Zellen in drei verschiedenen Fenstern der Embryonalentwicklung (zu Beginn, in der Mitte und am Ende). Diese Arbeit lieferte jedoch nur Momentaufnahmen der zellulären Vielfalt und Regulierung während bestimmter diskreter Zeitpunkte. Das Team untersuchte daher das Potenzial der Verwendung von Proben aus sich überschneidenden Zeitfenstern und wendete das Konzept zum Beweis des Prinzips auf eine bestimmte Zelllinie an - den Muskel.
Dies bildete dann die Grundlage für eine drastische Vergrößerung mit Hilfe einer neuen, im Shendure-Labor entwickelten Technologie. In der aktuellen Arbeit des Teams wurden Profile des offenen Chromatins von fast einer Million Zellen und der RNA von einer halben Million Zellen zu sich überschneidenden Zeitpunkten erstellt, die die gesamte Entwicklung des Fruchtfliegenembryos umfassen.
Mithilfe einer Art des maschinellen Lernens nutzten die Forscher die sich überschneidenden Zeitpunkte, um die Zeit mit einer viel feineren Auflösung vorherzusagen. Mitautor Diego Calderon, ein Postdoktorand im Shendure-Labor, trainierte ein neuronales Netz, um den genauen Entwicklungszeitpunkt für jede Zelle vorherzusagen.
"Obwohl die gesammelten Proben Embryonen mit leicht unterschiedlichem Alter innerhalb eines 2- oder 4-stündigen Zeitfensters enthielten, kann man mit dieser Methode jeden Teil dieser Zeitachse der Embryogenese auf einer Skala von Minuten heranzoomen", sagte Calderon.
Shendure fügte hinzu: "Ich war erstaunt, wie gut das funktioniert. Wir konnten molekulare Veränderungen erfassen, die sehr schnell, innerhalb von Minuten, ablaufen, was frühere Forscher durch die manuelle Auswahl von Embryonen alle drei Minuten aufgedeckt hatten.
In Zukunft wäre ein solcher Ansatz nicht nur zeitsparend, sondern könnte auch als Referenz für die normale Embryonalentwicklung dienen, um zu sehen, wie sich die Dinge bei verschiedenen mutierten Embryonen verändern. Auf diese Weise könnte genau festgestellt werden, wann und in welchem Zelltyp der Phänotyp einer Mutante auftritt, wie die Forscher im Muskel zeigten. Mit anderen Worten, diese Arbeit hilft nicht nur zu verstehen, wie die Entwicklung normalerweise abläuft, sondern öffnet auch die Tür zum Verständnis, wie verschiedene Mutationen sie durcheinander bringen können.
Das neue Vorhersagepotenzial, das diese Forschung auf der Grundlage von Proben aus viel größeren Zeitfenstern andeutet, könnte als Rahmen für andere Modellsysteme verwendet werden. Zum Beispiel für die Entwicklung von Säugetierembryonen, die In-vitro-Zelldifferenzierung oder sogar für die Zeit nach einer medikamentösen Behandlung kranker Zellen, wo die Lücken in den Probenahmezeiten so gestaltet werden können, dass sie eine optimale Zeitvorhersage mit einer geringeren Auflösung ermöglichen.
Für die Zukunft plant das Team, die Vorhersagekraft des Atlasses zu erforschen.
"Durch die Kombination all der neuen Werkzeuge, die uns in der Einzelzellgenomik, der Berechnung und der Gentechnik zur Verfügung stehen, würde ich gerne sehen, ob wir vorhersagen können, was mit einzelnen Zellschicksalen in vivo nach einer genetischen Mutation passiert", so Furlong. "...aber so weit sind wir noch nicht. Aber vor diesem Projekt dachte ich auch, dass die jetzige Arbeit nicht so bald möglich sein würde."
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Zellanalyse
Die Zellanalyse ermöglicht es uns, Zellen in ihren vielfältigen Facetten zu erforschen und zu verstehen. Von der Einzelzellanalyse über die Durchflusszytometrie bis hin zur Bildgebungstechnologie – die Zellanalyse bietet uns wertvolle Einblicke in die Struktur, Funktion und Interaktion von Zellen. Ob in der Medizin, der biologischen Forschung oder der Pharmakologie – die Zellanalyse revolutioniert unser Verständnis von Krankheiten, Entwicklung und Behandlungsmöglichkeiten.
Themenwelt Zellanalyse
Die Zellanalyse ermöglicht es uns, Zellen in ihren vielfältigen Facetten zu erforschen und zu verstehen. Von der Einzelzellanalyse über die Durchflusszytometrie bis hin zur Bildgebungstechnologie – die Zellanalyse bietet uns wertvolle Einblicke in die Struktur, Funktion und Interaktion von Zellen. Ob in der Medizin, der biologischen Forschung oder der Pharmakologie – die Zellanalyse revolutioniert unser Verständnis von Krankheiten, Entwicklung und Behandlungsmöglichkeiten.