Bisher unbekannter Modus des Bakterienwachstums entdeckt
Forschungsteam erklärt anhand von Bildgebung und Modellierungen, warum Bakterienzellen nicht immer exponentiell wachsen
Bakterien vermehren sich als einzellige Lebewesen durch die Teilung ihres gesamten Organismus. Auf diese Weise können sie sich besonders schnell reproduzieren, was das von Krankheitserregern bekannte exponentielle Wachstum von Bakterienpopulationen erlaubt. Dem Populationswachstum zugrunde liegt das individuelle Wachstum der einzelnen Bakterienzellen. Es ist ebenfalls durch eine schnelle Größenzunahme gekennzeichnet und je nach Art durch eine bestimmte maximale Zellgröße des ausgewachsenen Bakteriums limitiert. Bislang ging die Forschung davon aus, dass eine Bakterienzelle, genau wie ihre Population insgesamt, bis zum Erreichen dieser endgültigen Größe exponentiell wächst.
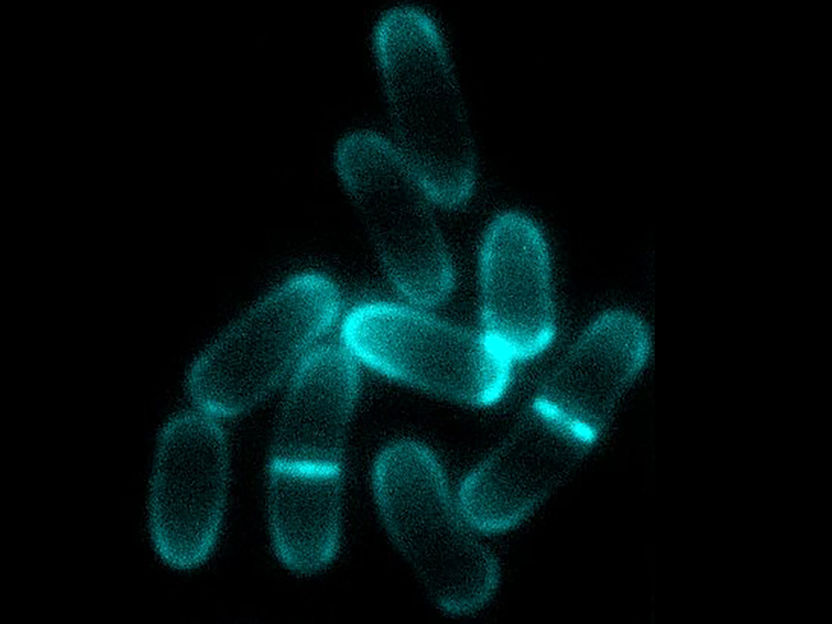
Am Modellorganismus Corynebacterium glutamicum lassen sich einerseits ungleich lange Tochterzellen und andererseits die Orte der Zellwandsynthese an den Zellpollen und der Teilungsebene gut erkennen.
© Fabian Meyer
An der Christian-Albrechts-Universität zu Kiel (CAU) beschäftigt sich die Arbeitsgruppe Mikrobielle Biochemie und Zellbiologie um Professor Marc Bramkamp unter anderem mit bakteriellen Organisations- und Reproduktionsmechanismen, deren allgemeingültige Prinzipien auch bei der Entstehung komplexer vielzelliger Lebewesen von Bedeutung sind. In einer neuen Forschungsarbeit konnten Bramkamp und sein Team vom CAU-Institut für Allgemeine Mikrobiologie am Beispiel des Bakteriums Corynebacterium glutamicum zeigen, dass Bakterien auch in einem anderen, nämlich zweistufigen Modus wachsen können: Corynebakterien wachsen durch die Synthese der Zellwand an den Zellpolen. Dabei ist die Wachstumsrate der Zellpole nach einer Zellteilung zunächst nicht identisch. Der jüngere Zellpol wächst direkt nach der Zellteilung zunächst langsamer. Aufgrund dieser besonderen Art der Zellverlängerung an den Zellpolen wachsen seine Zellen zunächst exponentiell und gehen dann in eine gleichmäßige, lineare Größenzunahme über. Auf Grundlage spezieller Bildgebungs- und eines neu entwickelten Analyseverfahrens gelang es den Forschenden, zunächst die Größenzunahme der Bakterienzellen im lebenden Organismus genau zu quantifizieren. Diese Daten flossen in theoretische Modellierungen ein, aus denen hervorging, dass der zweistufige Modus darauf zurückzuführen ist, dass die Zellwandbildung an den Polen der limitierende Prozess für das Wachstum von C. glutamicum ist. Die Ergebnisse veröffentlichten die Kieler Forschenden gemeinsam mit Kooperationspartnern an den Universitäten in Amsterdam und München in der wissenschaftlichen Fachzeitschrift eLife
Ungewöhnliches Bakterienwachstum beobachtet und modelliert
Die Regulation von Wachstum und Zellgröße ist entscheidend für die bakteriellen Zellfunktionen. Da man bislang davon ausging, dass Einzelzellen ihr Zellvolumen proportional zum steigenden Protein-Gehalt in ihrem Innern erhöhen müssen, nahm man bislang ein überwiegend exponentielles Wachstum an. Mit dieser schnellen Größenzunahme geht einher, dass Bakterien ihre Zellgröße streng kontrollieren müssen, um in ihrer Gestalt einheitliche Zellen in einer Population gewährleisten zu können. In der Tat verfügen viele Bakterienarten über komplexe Mechanismen zur Regulation ihrer Größe, bei C. glutamicum und den mit ihnen nahe verwandten Tuberkuloseerregern Mycobacterium tuberculosis, war ein solcher Mechanismus bisher aber nicht identifiziert worden.
Um die Besonderheit dieses bakteriellen Modellorganismus zu untersuchen, beobachtete das Kieler Forschungsteam sein Wachstum in vivo, also am lebenden Objekt. „Ein spannender Aspekt bei Corynebakterien, der bereits während der Mikroskopie sichtbar wird, ist, dass sich die Zellen nicht immer genau symmetrisch teilen, wie wir es von vielen anderen Bakterien kennen“, sagt Fabian Meyer, Doktorand in Bramkamps Gruppe. „Eine weitere Besonderheit ist, dass neue Zellwand hier nicht an der Längsseite der Zelle entsteht, sondern ausschließlich an den Zellpolen eingefügt wird“, erklärt Meyer. Daher werden diese Bakterien nur an den Zellenden verlängert und vergrößern ihr Volumen nicht wie viele andere Bakterien gleichmäßig über ihre gesamte Länge.
Um dieses ungewöhnliche Wachstumsverhalten von C. glutamicum charakterisieren zu können, entwickelte das Forschungsteam auf Grundlage der Kieler Daten ein theoretisches Modell der Größenentwicklung. Mit Hilfe von biophysikalischen Verfahren gelang es den Biophysikern Joris Messelink, Vrije Universiteit Amsterdam, und Professor Chase Broedersz von der Ludwig-Maximilians-Universität München, aus diesen Daten trotz des Messrauschens und der Variabilität von Zelle zu Zelle ein mittleres Dehnungsmuster der einzelnen Zelle im Zeitverlauf abzuleiten.
„Die Berechnungen zeigten, dass die Zellen zunächst immer schneller wachsen, dann aber in der Größenzunahme verlangsamt werden. Es ist also gewissermaßen eine Geschwindigkeitsbegrenzung in die Wachstumsdynamik von C. glutamicum eingebaut“, erklärt Broedersz. Im Gegensatz zum normalerweise exponentiellen Verlauf habe das Modell hier ein zweistufiges Wachstum der Bakterienzellen gezeigt, dass die Forschenden als asymptotisch linear bezeichnen. „Der limitierende Faktor für den Beginn des linearen Wachstums ist die Art der Zellwandbildung, die C. glutamicum von anderen Bakterien unterscheidet“, so Broedersz weiter. Diese theoretische Vorhersage konnte das Forschungsteam dann auch anhand von lebenden Bakterien bestätigen: Bei Bakterien, bei denen ein zentrales, aber redundantes Wachstumsenzym künstlich ausgeschaltet wurde, wodurch der begrenzende Faktor für das Zellwachstum verlangsamt wurde, wiederholten die Forschenden ihr Verfahren zur Wachstumsableitung. Die beobachteten Wachstumskurven zeigten eine allgemeine Abnahme der Dehnungsrate unter Beibehaltung der beiden Wachstumsstadien, was die theoretischen Vorhersagen bestätigte
Rückschlüsse auf die Bakterienevolution
"Die Modellierung des Zellwachstums sagt genau die Ergebnisse der In-vivo-Experimente voraus und rekapituliert die Besonderheiten des individuellen Zellwachstums in C. glutamicum. Darüber hinaus bieten die Ergebnisse eine evolutionäre Interpretation der Wachstumsmechanismen von C. glutamicum. Wie bei jedem Organismus müssen die bakteriellen Nachkommen der Elterngeneration in Größe und Form ähneln, und die Bakterien haben offenbar verschiedene Wachstumsstrategien entwickelt, um dieses Ziel zu erreichen“, fasst Bramkamp zentrale Erkenntnisse der interdisziplinären Kooperation von Forschenden aus der Zellbiologie und Biophysik zusammen. Bei Bakterien beziehe sich das vor allem auf die Zelllänge, deren Verteilung in einer Population relativ einheitlich sein sollte. „Unsere Ergebnisse zeigen, dass die Verteilung der Zelllängen beim asymptotischen linearen Wachstum enger ist als beim exponentiellen Wachstum. Der besondere Modus bei C. glutamicum, der in lineares Wachstum übergeht, könnte als Ersatz für eine strenge Regulierung der Teilungslänge dienen, da ein solches lineares Wachstum weniger empfindlich auf Schwankungen reagiert. Daher benötigt C. glutamicum möglicherweise keinen eigenen Mechanismus zur Wachstumskontrolle, wie wir ihn von anderen Bakterien kennen“, so Bramkamp weiter.