Innovativer Ansatz zur Zellbindung könnte unser Verständnis von Krankheiten verbessern
Die Liganden-Rezeptor-Bindung ist wichtig für biologische Prozesse wie Immunität und Infektionskrankheiten. Beispielsweise können Leukozyten durch Bindung an das P-Selektin auf den Endothelzellen in verletztes Gewebe eindringen. COVID-19 wird durch die Bindung zwischen viralen Spikes und Angiotensin-Converting Enzyme 2 (ACE2) auf den Wirtszellen verursacht. Zur Untersuchung der Bindungs- oder Adhäsionskinetik wurden verschiedene Arten von Einzelzelltests entwickelt.
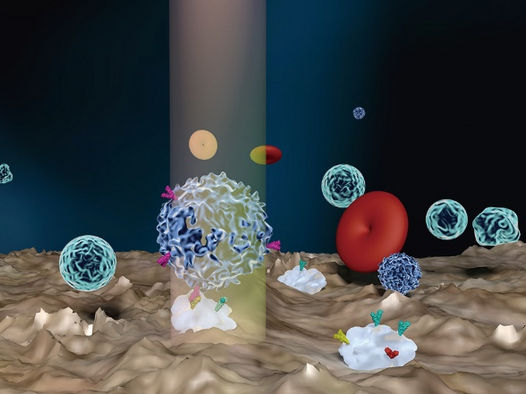
Der Einzelzell-Rotationsadhäsionsfrequenz-Assay (scRAFA) misst die Adhäsionskinetik von Zellen, die in der Nähe des Substrats eine lichtgesteuerte Rotation außerhalb der Ebene erfahren.
by Yaoran Liu, Ongru Ding, Jingang Li, Xin Lou, Mingcheng Yang, Yuebing Zheng
Die Unterschiede bei den gemessenen Bindungen zwischen P-Selektin und ACE2 sind jedoch bei allen Methoden erheblich. Dies ist darauf zurückzuführen, dass die gemessenen Proben unterschiedliche Längen der interagierenden Moleküle, der Linkermoleküle oder des Schemas der molekularen Immobilisierung aufweisen. Dies beeinflusst die Bindungsdissoziationskinetik. Bestehende Methoden messen die Zugkraft entlang der normalen Richtung der Zellgrenzfläche auf der Grundlage des Aufbrechens des Haftkontakts. Diese Methoden sind weit von den tatsächlichen Bedingungen der Zelladhäsion in vivo entfernt.
Die Zelladhäsionin vivo ist komplexer als das, was die bestehenden Methoden messen können. Zunächst wird eine Zelle in einer geneigten Richtung anhaften. Dann erfährt die Zelle eine durch die Flüssigkeitsströmung hervorgerufene Scherkraft, die es dem Rezeptor und dem Liganden ermöglicht, gegeneinander zu gleiten. Das Gleiten fördert die Bildung neuer Wechselwirkungen, nachdem die vorher bestehende Bindung abreißt. Die Kraftrichtung zwischen Ligand und Rezeptor ist tangential zur Zelle oder parallel zum Substrat, was zu einem unterschiedlichen Zelladhäsionsverhalten führt.
Vorläufige Studien haben gezeigt, dass Integrine eine laterale Kraft benötigen, um Zell-Zell-Wechselwirkungen zu vermitteln. T-Zell-Rezeptoren können eine tangentiale Kraft an der Kontaktfläche erzeugen. Mikrofluidische Kammern wurden angepasst, um diese Bedingung mit dem pumpengesteuerten Scherstrom zu untersuchen.
Mit den derzeitigen Techniken der Durchflusskammern lässt sich der Abstand zwischen Zelle und Substrat nicht genau steuern. Aufgrund der zufälligen Verteilung der Zellen in der Strömung können sie auch nicht auf eine bestimmte Zelle ausgerichtet werden. Es kann nur die Adhäsionskinetik eines Teils der Zellen analysiert werden, die unter der mikrofluidischen Strömung zufällige Rollprozesse durchlaufen. Es gibt keine Kontrolle der Adhäsionsmesszeit mit dem Durchflusskammertest. Diese Zeit entspricht in der Regel dem Zeitraum zwischen dem Kontakt der Zelle mit der Kammerwand und der ersten Bindung der Zelle an die Wand, wodurch die Genauigkeit der Zelladhäsionsanalyse eingeschränkt wird.
In einer neuen, in der Zeitschrift eLight veröffentlichten Arbeit untersuchte ein Team von Wissenschaftlern unter der Leitung von Professor Yuebing Zheng von der University of Texas in Austin die Steuerung von Zelloberflächenrezeptoren. Ihre Arbeit mit dem Titel "Light-driven single-cell rotational adhesion frequency assay" (Lichtgesteuerter Einzelzell-Rotationsadhäsionsfrequenztest) hat eine einzigartige Technik demonstriert, die den Ansatz der Wissenschaft in diesem Bereich dramatisch verändern könnte.
Sie ermöglichte die markierungsfreie und subzelluläre Quantifizierung der Adhäsion fast aller gezielten Einzelzellen in klinischen Lösungen. Mit scRAFA hat das Team die Adhäsionskräfte von Zellen gemessen, die in der Nähe des Substrats eine lichtgetriebene Rotation außerhalb der Ebene erfahren. Ihr Ansatz unterscheidet sich deutlich von der herkömmlichen Messung der Adhäsionskinetik durch Aufbrechen des Haftkontakts in normaler Richtung,
Die Forscher zielen auf spezifische Zellen durch eine nahtlose Fusion von optischer Rotation und Einfangen auf einer einzigen Plattform. Dadurch konnte das Team den gesamten Prozess der Zelladhäsion kontinuierlich überwachen, vom Beginn der Bindung an das Substrat bis zur Bildung der dauerhaften Verbindung. Außerdem konnten sie den Interaktionsabstand zwischen den Substratliganden und den Zellrezeptoren präzise steuern, um erstmals die Kinetik der lateralen Adhäsion zu messen. Somit ermöglicht scRAFA hochpräzise In-situ-Messungen der Scheradhäsionskräfte an Zielzellen in komplexen klinischen Proben.
Das lichtgesteuerte scRAFA verfügt über eine Reihe von Funktionen, die in einem einzigen System integriert sind, darunter optisches Trapping, Rotation, Bildgebung und Spektroskopie. Ihr scRAFA kann gezielt Organismen in komplexen Flüssigkeiten für die Adhäsionsmessung lokalisieren. Es kann auch zusätzliche optische Charakterisierungen der Strukturen und anderer Funktionen der Organismen ermitteln. Diese Funktionalität vereinfacht die Erstellung vollständiger Struktur-Funktions-Beziehungen auf der Ebene des einzelnen Organismus.
Rotationsadhäsions- und Scherkraftmessungen für Zellen mit homogenen und heterogenen Oberflächen. Die Fähigkeit, die strukturelle und funktionelle Heterogenität von Einzelzellen aufzudecken, ist entscheidend für die Untersuchung von zellulären Mikrodomänen, Clustern und Tether. Ihre Adhäsionsanalyse ist auch für das Verständnis von Immunreaktionen und bakteriellen Infektionen von großer Bedeutung.
Am wichtigsten ist jedoch, dass ihr scRAFA auf Organismen unter verschiedenen physiologischen Bedingungen angewendet werden kann. Es kann sogar das von der Scherkraft abhängige Adhäsionsverhalten aufzeigen, da die Laserleistung die Strömung und das Rotationsmoment der Flüssigkeit einstellt. Die erste Studie zeigte, dass ihr scRAFA das Adhäsionsverhalten zwischen kultivierten Hefezellen und solchen in klinischen Proben unterscheiden kann.
Für eine breitere Anwendung des scRAFA ist eine weitere Modellierung der Organismen und ihrer Interaktionen mit Substraten erforderlich. Mit seiner überragenden Leistung und allgemeinen Anwendbarkeit könnte scRAFA eine entscheidende Rolle in Bereichen von der Zellbiologie über die Immuntherapie bis hin zu Harnwegsinfektionen spielen.
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.