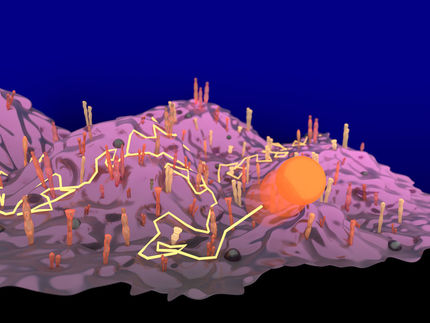
Sehen mit den grauen Zellen: Neue Mikroskopie-Methode macht Nervenschaltungen im Gehirn sichtbar
Wenn sich ein Gegenstand vor unserem Auge bewegt, feuern bestimmte Nervenzellen in unserem Hinterkopf elektrische Signale - je nach Bewegungsrichtung sind andere Zellen aktiv. Wissenschaftler der Technischen Universität München (TUM) können jetzt im Gehirn beobachten, wie einzelne dieser Nervenzellen solche Bewegungssignale empfangen und verarbeiten: Erstmals kann eine neue Mikroskopie-Methode einzelne, ein Tausendstel Millimeter kleine Nervenverschaltungen (Synapsen) darstellen. In Zukunft könnte die Methode verstehen helfen, wie Lernen auf der Ebene einer Nervenzelle funktioniert.
Licht, das auf die Netzhaut des menschlichen Auges fällt, trifft dort auf 126 Millionen Sinneszellen, die es in elektrische Signale umwandeln. Bereits die kleinste Einheit des Lichts, ein Photon, kann eine der Sinneszellen stimulieren. Die Folge: Ungeheure Datenmengen müssen verarbeitet werden, damit wir sehen können. Die Datenverarbeitung beginnt bereits in der Netzhaut, aber das fertige Bild entsteht erst im Gehirn, genauer: in der Sehrinde im hinteren Teil des Großhirns.
Die Wissenschaftler um den TUM-Neurophysiologen Prof. Arthur Konnerth interessieren sich für eine bestimmte Sorte von Nervenzellen in der Sehrinde, die auf Bewegungen reagiert. Ob vor dem Auge ein Balken von unten nach oben wandert oder von rechts nach links: Stets reagieren andere Nervenzellen der Sehrinde. Wie die gesendeten Impulse dieser "Richtungs"-Neuronen aussehen, ist gut bekannt - doch wie sieht das Eingangssignal aus? Das ist nicht leicht zu beantworten, denn jede der Nervenzellen besitzt einen ganzen Baum winziger, verästelter Antennen, an die hunderte anderer Nervenzellen mit ihren Synapsen andocken.
Um mehr über das Eingangssignal herauszufinden, schauten Konnerth und seine Mitarbeiter einer Maus beim Sehen zu. Dazu verfeinerten sie eine Mikroskopie-Methode, mit der sich bis zu einem halben Millimeter in das Hirngewebe hineinblicken und eine einzelne Zelle beobachten lässt, die sogenannte 2-Photonen-Fluoreszenz-Mikroskopie. Gleichzeitig leiteten sie mit haarfeinen Pipetten elektrische Signale an einzelnen Baum-Fortsätzen derselben Nervenzelle ab (Patch-Clamp-Technik). Konnerth: "Ähnliche Versuche wurden bisher nur in Kulturschalen mit gezüchteten Nervenzellen gemacht, lebendes Gewebe ist viel komplexer. Da es sich immer ein bisschen bewegt, war es sehr schwierig, alle Verästelungen eines Neurons im Bild so hoch aufzulösen, dass wir einzelne Synapsen darstellen konnten."
Der Lohn der Anstrengungen: Konnerth und seine Kollegen entdeckten, dass ein "Richtungs"-Neuron bei mehreren, unterschiedlichen Bewegungen des Balkens vor dem Auge Signale von den mit ihm vernetzten Nervenzellen empfängt. "Hier wird es richtig spannend", meint Konnerth. Denn die "Richtungs"-Nervenzelle versendet nur ein Ausgangssignal wie zum Beispiel "bewegt sich von unten nach oben". Offenbar verrechnet sie also die unterschiedlichen Eingangssignale miteinander und reduziert damit die Fülle eintreffender Einzeldaten auf wesentliche Informationen, die für das klare Sehen einer Bewegung wichtig sind.
In Zukunft will Konnerth mit seinem Forschungsansatz auch den Prozess des Lernens an einer einzelnen Nervenzelle beobachten. Viele Nervenenden senden praktisch nie Signale an den Antennen-Baum eines "Richtungs"-Neurons. Wenn das Auge etwa andere Arten von Bewegungen wahrnimmt, könnten solche stummen Nervenenden aktiv werden. Das würde den Verrechnungsmechanismus der "Richtungs"-Nervenzelle so verändern, dass sie ihre bevorzugte Richtung ändert: Die Maus würde lernen, bestimmte Bewegungen vielleicht besser oder schneller zu sehen. "Da wir mit unserer Methode gleichzeitig die Verschaltung und das Verhalten ein und derselben Nervenzelle im Gehirn beobachten können, werden wir einen wichtigen Beitrag zum Verständnis von Lernen leisten können", ist Konnerth überzeugt. "Hier an der TU München arbeiten wir eng mit Physikern und Ingenieuren zusammen. So haben wir beste Chancen, die räumliche und zeitliche Auflösung der Bilder weiter zu verbessern."
Originalveröffentlichung: Hongbo Jia, Nathalie L. Rochefort, Xiaowei Chen, Arthur Konnerth; "Dendritic organization of sensory input to cortical neurons in vivo"; Nature 464, 1307-1312 (29 April 2010)
Meistgelesene News
Themen
Organisationen
Weitere News aus dem Ressort Wissenschaft
Diese Produkte könnten Sie interessieren

Holen Sie sich die Analytik- und Labortechnik-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Pipettieren
Pipettieren ist eine der grundlegendsten und dennoch kritischsten Techniken im Labor. Es ermöglicht das präzise und kontrollierte Übertragen von Flüssigkeiten, was für genaue Messungen und zuverlässige Ergebnisse unerlässlich ist. Ob bei der DNA-Analyse, der Zellkultur oder biochemischen Assays – das korrekte Pipettieren beeinflusst maßgeblich die Qualität der Ergebnisse.

Themenwelt Pipettieren
Pipettieren ist eine der grundlegendsten und dennoch kritischsten Techniken im Labor. Es ermöglicht das präzise und kontrollierte Übertragen von Flüssigkeiten, was für genaue Messungen und zuverlässige Ergebnisse unerlässlich ist. Ob bei der DNA-Analyse, der Zellkultur oder biochemischen Assays – das korrekte Pipettieren beeinflusst maßgeblich die Qualität der Ergebnisse.
Themenwelt Fluoreszenzmikroskopie
Die Fluoreszenzmikroskopie hat die Life Sciences, Biotechnologie und Pharmazie revolutioniert. Mit ihrer Fähigkeit, spezifische Moleküle und Strukturen in Zellen und Geweben durch fluoreszierende Marker sichtbar zu machen, bietet sie einzigartige Einblicke auf molekularer und zellulärer Ebene. Durch ihre hohe Sensitivität und Auflösung erleichtert die Fluoreszenzmikroskopie das Verständnis komplexer biologischer Prozesse und treibt Innovationen in Therapie und Diagnostik voran.
Themenwelt Fluoreszenzmikroskopie
Die Fluoreszenzmikroskopie hat die Life Sciences, Biotechnologie und Pharmazie revolutioniert. Mit ihrer Fähigkeit, spezifische Moleküle und Strukturen in Zellen und Geweben durch fluoreszierende Marker sichtbar zu machen, bietet sie einzigartige Einblicke auf molekularer und zellulärer Ebene. Durch ihre hohe Sensitivität und Auflösung erleichtert die Fluoreszenzmikroskopie das Verständnis komplexer biologischer Prozesse und treibt Innovationen in Therapie und Diagnostik voran.