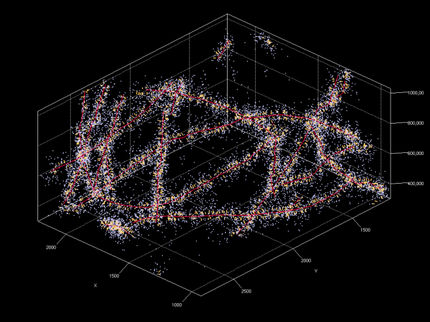
Neue Mikroskopie-Methode löst Fluoreszenzmoleküle nanometergenau auf
Wissenschaftler um Stefan Hell vom Göttinger Max-Planck-Institut (MPI) für biophysikalische Chemie und dem Heidelberger MPI für medizinische Forschung haben eine neue Lichtmikroskopie-Methode entwickelt, MINSTED genannt. Sie trennt fluoreszenzmarkierte Details mit molekularer Schärfe. Für Nobelpreisträger Hell schließt sich damit ein Kreis.
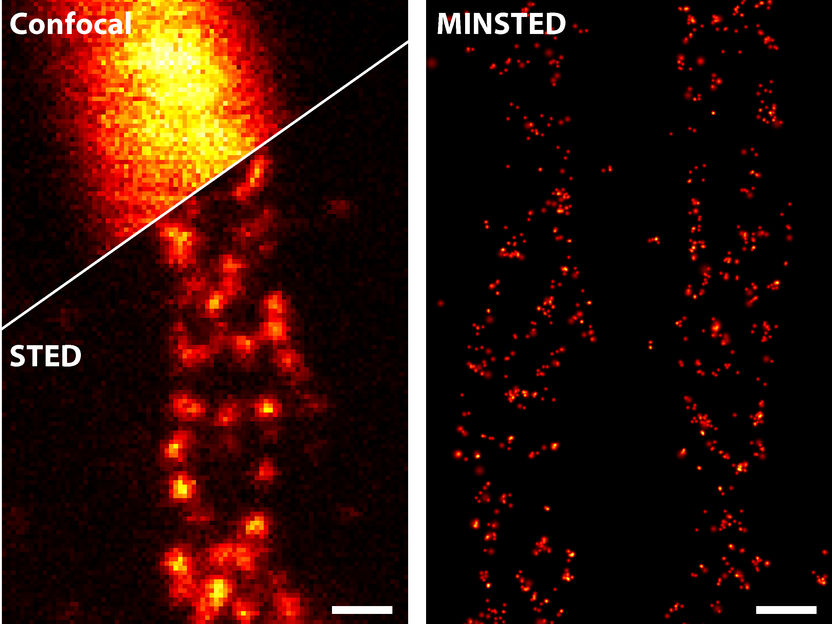
Verschiedene lichtmikroskopische Techniken im Vergleich: Bereits STED (links unten) verbessert die Detailschärfe gegenüber herkömmlicher konfokaler Mikroskopie (links oben) drastisch. MINSTED (rechts) erreicht eine noch mal zehnfach höhere Auflösung.
© Michael Weber / Max-Planck-Institut für biophysikalische Chemie
„Vor gut 20 Jahren haben wir mit der STED-Mikroskopie die Beugungsgrenze des Lichts in der Fluoreszenz-Lichtmikroskopie grundlegend durchbrochen. Das galt bis dahin als unmöglich,“ so Hell. „Damals haben wir geträumt: STED soll eines Tages so gut werden, dass man damit einzelne Moleküle trennen kann, die nur ein paar Nanometer voneinander entfernt sind. Jetzt ist uns das gelungen.“ Das STED-Prinzip kam damals einer Revolution in der Lichtmikroskopie gleich. Dafür erhielt Hell 2014 den Nobelpreis für Chemie.
In seiner ursprünglichen Fassung erreicht die STED-Mikroskopie eine Trennschärfe von bis zu 20 bis 30 Nanometern (Millionstel Millimeter) und ist damit etwa zehn Mal schärfer als die bis dahin verfügbaren Lichtmikroskope. 2016 konnten Hell und seine Mitarbeiter die Auflösung noch einmal um das Zehnfache steigern: Für die sogenannte MINFLUX-Nanoskopie kombinierten sie ein Element aus dem STED-Prinzip mit einem aus einer anderen Mikroskopie-Technik, PALM/STORM, und erreichten so erstmals eine Trennschärfe von wenigen Nanometern. MINFLUX kann Fluoreszenzmoleküle auf molekularen Skalen sichtbar machen – schärfer geht es nicht mehr.
Eine ganze Familie von Fluoreszenzmikroskopen
MINFLUX wird aber nicht die einzige molekular auflösende Methode bleiben, sondern verkörpert nur das erste Beispiel für eine neue Familie von Fluoreszenzmikroskopen, die bis auf molekulare Skalen vordringen können – davon war Hell überzeugt. Mit MINSTED liefern seine Mitarbeiter und er jetzt den Beweis dafür. Wie der Name schon sagt, trägt MINSTED noch mehr als MINFLUX vom ursprünglichen STED-Prinzip in sich. „Und das bringt Vorteile,“ sagt Michael Weber, Doktorand in Hells Labor. „Es erreicht wie MINFLUX molekulare Auflösung, aber das Hintergrundrauschen ist geringer. Hinzu kommt, dass man die Auflösung von 200 Nanometern bis hinunter zur Molekülgröße – 1 Nanometer – nun fast stufenlos einstellen kann.“
Mit MINSTED knüpft Hell so an seinen gut 20 Jahre zurückliegenden Durchbruch mit STED an und schöpft das volle Potenzial dieser Technik aus. „Mikroskopie auf molekularer Skala ist somit auf eine breite physikalische Basis gestellt. Es ist zu erwarten, dass MINSTED und MINFLUX grundlegende Verfahren werden, die in den Lebenswissenschaften vielfach Anwendung finden“, so der Physiker.
Das Leuchten von Molekülen an- und ausschalten
STED erreichte das zuvor Unerreichte – weniger als 200 Nanometer voneinander entfernte Moleküle getrennt zu erfassen – mit einem Trick: benachbarte fluoreszierende Moleküle werden nacheinander an- und ausgeschaltet. Dafür schickt das STED-Mikroskop einem die Moleküle anregenden Laserstrahl einen zweiten hinterher, den sogenannten STED-Strahl, der die Moleküle am Fluoreszieren hindert. Der STED-Strahl hat aber in der Mitte ein „Loch“; er ist also Donut-förmig. Nur die Moleküle in der Mitte dieses Donutstrahls können somit leuchten. Daher weiß man immer, wo sich die leuchtenden Moleküle befinden. STED erreicht in der Praxis allerdings keine molekulare Auflösung, weil sich der Donutstrahl, der das Leuchten unterdrückt, nicht so stark machen lässt, dass nur noch ein einziges Molekül ins Loch passt.
Deshalb werden bei MINSTED die Fluoreszenzmoleküle erst einmal vereinzelt und räumlich verstreut ein- und ausgeschaltet, und zwar nicht mit dem STED-Donutstrahl sondern über einen photochemischen Schaltprozess. Den STED-Donutstrahl benutzt man aber dazu, die Fluoreszenzmoleküle einzeln zu orten. Dabei dient sein Loch als Referenzpunkt. „Fällt das Loch mit dem Molekül zusammen, so leuchtet dieses am stärksten und man weiß genau, wo es ist. Denn die Position des STED-Donutstrahls ist elektronisch gesteuert und damit genau bekannt,“ erklärt Marcel Leutenegger, Postdoktorand in Hells Abteilung. „Deshalb tasten wir uns mit dem Donutstrahl kreisend an die Moleküle heran und können sie so mit einer Genauigkeit von 1 bis 3 Nanometern – also Molekülgröße – orten. In Verbindung mit dem photochemischen Ein- und Ausschalten wird die Auflösung molekular.“
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Fluoreszenzmikroskopie
Die Fluoreszenzmikroskopie hat die Life Sciences, Biotechnologie und Pharmazie revolutioniert. Mit ihrer Fähigkeit, spezifische Moleküle und Strukturen in Zellen und Geweben durch fluoreszierende Marker sichtbar zu machen, bietet sie einzigartige Einblicke auf molekularer und zellulärer Ebene. Durch ihre hohe Sensitivität und Auflösung erleichtert die Fluoreszenzmikroskopie das Verständnis komplexer biologischer Prozesse und treibt Innovationen in Therapie und Diagnostik voran.
Themenwelt Fluoreszenzmikroskopie
Die Fluoreszenzmikroskopie hat die Life Sciences, Biotechnologie und Pharmazie revolutioniert. Mit ihrer Fähigkeit, spezifische Moleküle und Strukturen in Zellen und Geweben durch fluoreszierende Marker sichtbar zu machen, bietet sie einzigartige Einblicke auf molekularer und zellulärer Ebene. Durch ihre hohe Sensitivität und Auflösung erleichtert die Fluoreszenzmikroskopie das Verständnis komplexer biologischer Prozesse und treibt Innovationen in Therapie und Diagnostik voran.