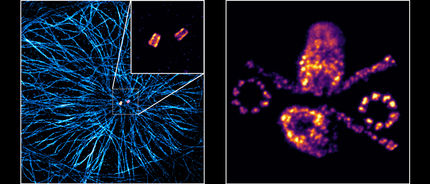
Verkehrskontrolle für Zellen
Forscher entwickeln Hydrogel, dessen Steifigkeit und Durchlässigkeit für Zellen mit Licht kontrollierbar ist
Zellen im menschlichen Körper können sich unterschiedlich verhalten, abhängig von den mechanischen Eigenschaften des Gewebes, das sie umgibt. Dies gilt besonders für Immunzellen, die durch den Körper wandern, dabei auf Gewebe mit unterschiedlichen Eigenschaften treffen und darauf angemessen reagieren müssen. Um Untersuchungen zu ermöglichen, wie Zellen sich verhalten, wenn sich die Steifigkeit des umgebenden Gewebes verändert, haben sich Wissenschaftler der Freiburger Exzellenzcluster im Bereich biologische Signalforschung BIOSS und CIBSS sowie des Exzellenzclusters livMatS zusammengetan: Sie haben als zelluläre Umgebung ein Hydrogel entwickelt, dessen Steifigkeit sie mithilfe von Lichtsignalen erhöhen und senken können.
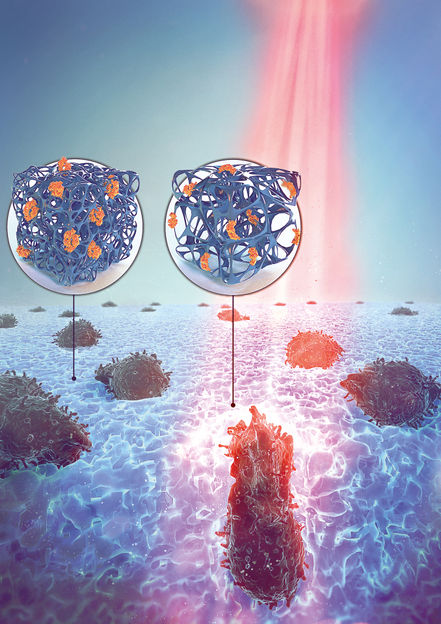
Jo Richers
In der Optogenetik nutzen Forscher Licht, um zelluläre Proteine und Prozesse präzise zu steuern. Bislang hat sich die Anwendung vor allem auf Vorgänge innerhalb der Zelle konzentriert. „Werkzeuge, die es erlauben, die Eigenschaften der zellulären Umgebung räumlich und zeitlich genau zu kontrollieren, fehlen bisher weitgehend“, sagt Prof. Dr. Wilfried Weber, Hauptautor der Studie und Mitglied des Sprecherteams von CIBSS – Centre for Integrative Biological Signalling Studies. „Unsere Forschung zeigt aber, dass von der Optogenetik inspirierte Ansätze vielversprechende Möglichkeiten eröffnen, mit denen wir analysieren können, wie Zellen auf Veränderungen in ihrer Umgebung reagieren.“
Um ein Hydrogel zu entwickeln, dessen Steifigkeit sich mithilfe von Lichtsignalen erhöhen und senken lässt, war es zunächst erforderlich, einen passenden molekularen Schalter zu finden. Nach Recherche in ihrer öffentlich zugänglichen Datenbank OptoBase entschieden sich die Autoren für das Protein Cph1 – ein Phytochrom, das in Bakterien vorkommt und auf Licht reagiert: Wird es hellrotem Licht ausgesetzt, bindet es an ein anderes Cph1-Molekül, bei dunkelrotem Licht wird diese Bindung wieder gelöst.
Die Wissenschaftler entwickelten eine Variante von Cph1 mit eingebauten Andockstellen für Zellen. Dieses Protein koppelten sie an ein verzweigtes Polyethylenglykol-Polymer und stellten damit ein Hydrogel her. Wird es hellrotem Licht ausgesetzt, binden die enthaltenen Cph1-Moleküle aneinander und erhöhen so die Quervernetzung und damit die Steifigkeit des Hydrogels; bei dunkelrotem Licht lösen sich die Bindungen, und die Steifigkeit wird wieder verringert. Die Gruppe von Prof. Dr. Andreas Walther vom Exzellenzcluster livMatS – Living, Adaptive and Energy-autonomous Materials Systems war an der Bestimmung von physikalischen Eigenschaften des Hydrogels, die eine entscheidende Rolle für die Zellmigration spielen, unter verschiedenen Beleuchtungsbedingungen beteiligt. „Dieses System ist ideal, um zu erforschen, wie Zellen auf dynamische Veränderungen der mechanischen Eigenschaften ihrer Umgebung reagieren“, erklärt Dr. Maximilian Hörner, Erstautor der Studie. „Wir können die Materialeigenschaften in Sekundenschnelle beeinflussen, wobei die Veränderungen vollständig umkehrbar und präzise regulierbar sind.“
In Experimenten zur Wanderung von T-Zellen, einem Typ von Immunzellen, der Krebs bekämpfen kann, zeigten die Autoren: Nur diejenigen Teile der Matrix, die dunkelrotem Licht ausgesetzt waren und daher eine geringere Steifigkeit aufwiesen, waren durchlässig für die Wanderung von T-Zellen. „Wir beobachteten, dass T-Zellen, die Tumore bekämpfen können, nicht durch eine Matrix mit erhöhter Steifigkeit wandern können. Zugleich ist bekannt, dass Tumorzellen bevorzugt durch steifes Gewebe wandern, um die Invasion und Bildung von Metastasen auszulösen“, sagt Gruppenleiterin Privatdozentin Dr. Susana Minguet, die an der Studie ebenfalls beteiligt war. „Die kontrollierbare Matrix imitiert die sich dynamisch verändernden Umgebungen, denen Immunzellen begegnen, wenn sie sich durch gesundes Gewebe oder Tumorgewebe bewegen. Damit hat sie das Potenzial, zu erklären, warum manche auf T-Zellen basierende Immuntherapien gegen Krebs nicht erfolgreich sind, und zur Entwicklung besserer therapeutischer Ansätze beizutragen.“
Originalveröffentlichung
Hörner M., Raute K., Hummel B., Madl J., Creusen G., Thomas O.S., Christen E.H., Hotz N., Gübeli R.J., Engesser R., Rebmann B., Lauer J., Rolauffs B., Timmer J., Schamel W.W.A., Pruszak J., Römer W., Zurbriggen M.D., Friedrich C., Walther A., Minguet S., Sawarkar R. and Weber W.; "Phytochrome-Based Extracellular Matrix with Reversibly Tunable Mechanical Properties"; Advanced Materials; 2019, 31(12):e1806727.
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Zellanalyse
Die Zellanalyse ermöglicht es uns, Zellen in ihren vielfältigen Facetten zu erforschen und zu verstehen. Von der Einzelzellanalyse über die Durchflusszytometrie bis hin zur Bildgebungstechnologie – die Zellanalyse bietet uns wertvolle Einblicke in die Struktur, Funktion und Interaktion von Zellen. Ob in der Medizin, der biologischen Forschung oder der Pharmakologie – die Zellanalyse revolutioniert unser Verständnis von Krankheiten, Entwicklung und Behandlungsmöglichkeiten.
Themenwelt Zellanalyse
Die Zellanalyse ermöglicht es uns, Zellen in ihren vielfältigen Facetten zu erforschen und zu verstehen. Von der Einzelzellanalyse über die Durchflusszytometrie bis hin zur Bildgebungstechnologie – die Zellanalyse bietet uns wertvolle Einblicke in die Struktur, Funktion und Interaktion von Zellen. Ob in der Medizin, der biologischen Forschung oder der Pharmakologie – die Zellanalyse revolutioniert unser Verständnis von Krankheiten, Entwicklung und Behandlungsmöglichkeiten.