Verbotene FRET-Zustände auf hauchdünnem Gold
Aktivierung G-Protein-gekoppelter Rezeptoren detaillierter untersuchen
G-Protein-gekoppelte Rezeptoren (GPCR) sind die wichtigsten Zielmoleküle für die Arzneiforschung. Wissenschaftlern der Universität Würzburg und des Universitätsklinikums Jena ist es jetzt durch moderne Mikroskopieverfahren gelungen, die Aktivierung dieser Rezeptoren detaillierter zu untersuchen. Die Verstärkung des Förster-Resonanzenergietransfers (FRET) durch den Einsatz speziell beschichteter Deckgläser war der Schlüssel dazu.
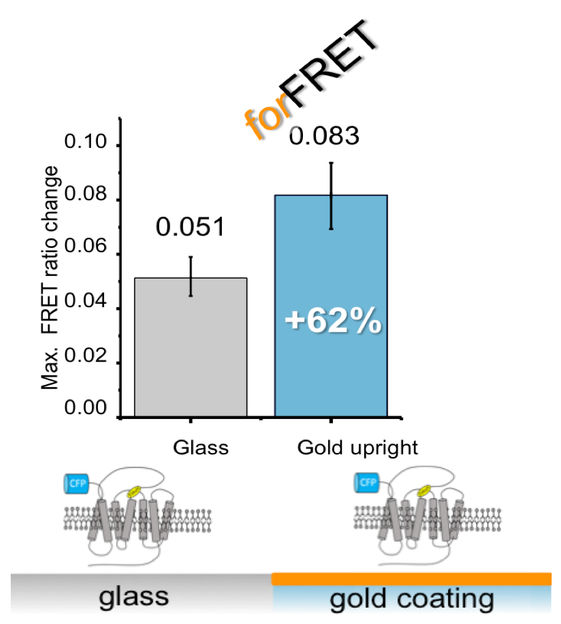
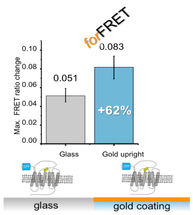
Auf beschichteten Deckgläsern kann um 62% erhöhte dynamische FRET-Antwort zwischen den inaktiven und aktiven Zuständen beobachtet werden.
Rudolf-Virchow-Zentrum
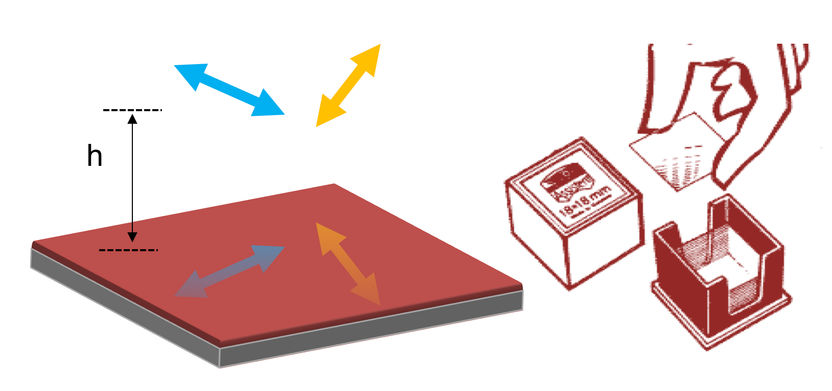
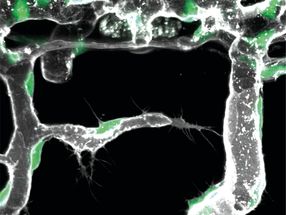
Goldbeschichtung von wenigen Nanometern kann ein sonst herkömmliches Deckglas in Verstärker verwandeln. Die Beschichtung ist biokompatibel und für die Kultivierung von adhärenten Zellen geeignet.
Rudolf-Virchow-Zentrum
Diese neue Methode könnte sowohl Einzelzellmessungen zu mehr Präzision verhelfen, als auch Hochdurchsatz-Screenings optimieren, welche für die Medikamentenentwicklung eine große Rolle spielen.
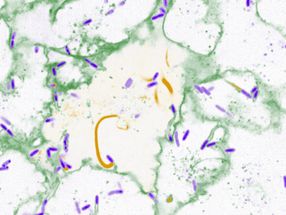
Will man die Konformationsänderung oder Interaktion von Membranrezeptoren in lebenden Zellen beobachten, sind lichtmikroskopische Verfahren oft die Methode der Wahl. Ein Phänomen, was das Auslesen dieser Änderungen und Interaktionen erlaubt, ist der sogenannte Förster-Resonanzenergietransfer (FRET). Dieser erscheint immer dann, wenn sich zwei Fluorophore mit geeigneten spektralen Eigenschaften räumlich sehr nah kommen, und in korrekter Orientierung zueinander stehen.
Jedes Photon zählt
FRET dient als molekulares Lineal zwischen zwei Molekülen oder molekularen Kompartimenten. Die Methode ist leistungsstark, hat aber oft durch die begrenzte Anzahl der emittierten Photonen ihre Grenzen. Es macht das Design und die Etablierung eines entsprechenden FRET-Paares schwierig und fehleranfällig. In biologischen Untersuchungen ist es besonders schwierig, die Nähe und Orientierung der Fluorophore zu optimieren, ohne die physiologischen Eigenschaften des molekularen Komplexes zu stören.
Spiegeleffekt erlaubt „verbotene“ Zustände
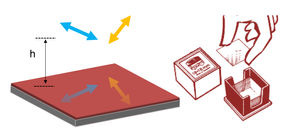
Die Forscherteams der Professorin Katrin Heinze und des Professors Carsten Hoffmann haben nun die Hürden für die Nutzung der FRET Methode gesenkt. Die Forschungsgruppen haben nanobeschichtete Deckgläser verwendet, die mit speziellen Goldbeschichtungen versehen sind. Diese biokompatiblen Deckgläser bewirken eine Verstärkung des Energieübertrags, besonders für suboptimal orientierte FRET-Paare. Dies geschieht unter anderem dadurch, dass das FRET-Paar durch die Goldbeschichtung sich selbst im Spiegel „sieht“. Dadurch stehen komplementäre Orientierungen für den Energieübertrag zur Verfügung, die den „Netto“-FRET erhöhen. Der Spiegeleffekt erlaubt also die Abfrage sonst „verbotener“ Zustände für FRET. Physikalisch bezeichnet man diesen Effekt als Depolarisation, hervorgerufen durch das komplexe Reflexionsverhalten des FRET-Paares nahe der Goldoberfläche.
Lange Zeit war es unter Physikern umstritten, ob es eine ausreichend starke FRET Erhöhung geben kann; dabei wurde die Orientierung der Moleküle nie ausreichend beachtet. Neueste theoretische und experimentelle Arbeiten an physikalischen Systemen gaben aber Anlass, die Möglichkeit der FRET-Verstärkung nochmal aufzugreifen.
„Diskussionen mit anderen Experten im Forschungsfeld stimmten uns zunächst nur vorsichtig optimistisch. Unsere Simulationen für den FRET Sensor des M1-Acetylcholin-Rezeptors zeigten allerdings, dass eine FRET-Verstärkung sehr wahrscheinlich ist. Die Experimente bestätigten schließlich in der Tat genau unsere Vorhersagen. So entstand unser „forbiddenFRET (forFRET)“, sagt Katrin Heinze. Carsten Hoffmann fügt hinzu: „ Diese Technologie ist zwar erst ganz am Anfang, aber sie hat großes Potential die Untersuchungen von GPCR Aktivierungen und Interaktionen in Zukunft noch exakter zu gestalten.“
Originalveröffentlichung
Schreiber, Benjamin; Kauk, Michael; Heil, Hannah; Emmerling, Monika; Tessmer, Ingrid; Kamp, Martin; Höfling, Sven; Holzgrabe, Ulrike; Hoffmann, Carsten; Heinze, Katrin; "Enhanced fluorescence resonance energy transfer in G protein-coupled receptor probes by nano-coated microscopy coverslips"; ACS Photonics; March 2018